양성 종양과 악성 종양의 차이
| 양성 종양 | 악성 종양 | |
| 성장 속도 | 천천히 자라며, 성장이 멈추는 휴지기가 나타날 수 있음 | 빠르게 자라며 저절로 없어지는 경우는 거의 없음 |
| 세포 특징 | 세포가 잘 분화되어 있어 대부분 고유의 기능을 유지 | 세포가 탈분화되어 있는 미성숙 상태로, 고유의 기능을 잃음 ex) Teratoma |
| 성장 양식 | 피막에 싸여 있어 주변 조직과 구분됨 | 피막이 없어 주변 조직을 침범하며 성장 |
| 전이 여부 | 혈관이나 림프관을 침범하지 않아 전이가 거의 없음 | 혈관이나 림프관 침범 후 전신으로 전이될 수 있음 |
| 재발 여부 | 경계가 뚜렷해 수술로 제거가 용이하며 재발이 거의 없음 | 주변 조직에 침투해 자라기 때문에 수술이 어려움 |
| 예후 | 생명을 위협하는 경우는 거의 없음 | 종양 크기, 림프절 침범 여부, 전이 유무 등에 따라 달라짐 |
암
1. 암의 특징
- 분열 조절이 안 됨
- 밀도 의존적 억제가 되지 않음 (와버그 효과 : 산소 고갈 시 젖산 발효)
- 인테그린, 캐드히린 등의 발현이 감소해 부착 비의존적으로 변하고 세포 골격도 느슨해짐
- 주변 조직으로 침투
- 새로운 혈관을 형성(Angiogenesis)
- 고유의 기능을 잃고 탈분화된 미성숙 상태로 바뀜
- 혈관이나 림프관을 따라 주변 조직으로 전이될 수 있음 (암환자는 림프절을 제거하기도 함)
- 스스로 성장 인자를 방출해 증식
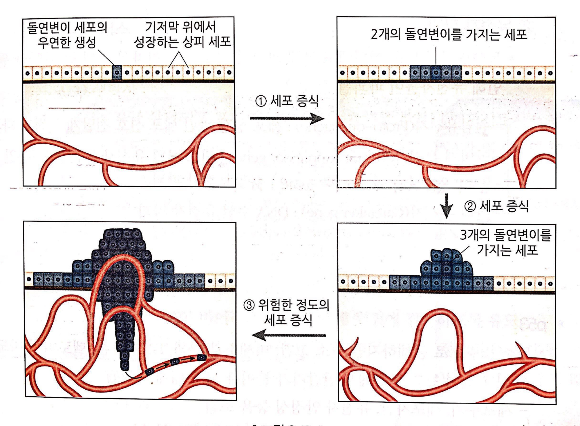
2. 암의 원인
1) 돌연변이 물질
다양한 돌 연변 이원들이 DNA의 구조 변성 및 염기 이상을 유발
-체 내에서 해독할 때 시토크롬 P450에 의해 산화되면서 더 큰 반응성을 띄게 되기도 함
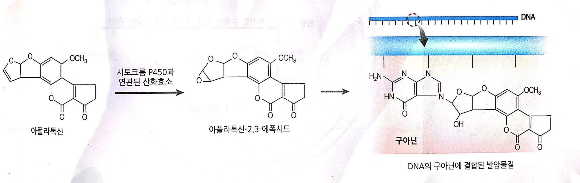
2) 유전자 파괴
돌연변이원 노출 이외에도 복제 과정의 실수, 전이인자의 전위 등 다양한 원인들로 인해 유전자들이 파괴될 수 있음
-원암 유전자 : 세포 성장 관련 세포 신호 전달계 유전자 파괴
-암 억제 유전자
-> 문지기 유전자 : 세포 사멸 유전자 또는 세포 분열 조절 유전자 파괴
-> 관리 유전자 : DNA 수선 유전자 파괴
3) 종양 바이러스
(i) DNA 바이러스 - 인간 유두종 바이러스(HPV)
(ㄱ) 생활사
- 자궁 상피세포 표면의 헤파린을 수용체로 부착해 엔도시토시스 됨
- 엔도좀이 산성 pH가 되면 캡시드가 제거되고 DNA만 빠져나와 핵 속으로 들어감
- 숙주의 RNA 합성효소 II를 이용해 전기 프로모터로부터 유전자가 전사됨
- 전사체는 선택적 스플라이싱을 통해 여러 가지 mRNA를 생성해서 E1~E7 단백질로 번역됨 (E1 : 헬리케이즈 활성 E2 : E1이 바이러스 DNA의 복제 원점에 결합하도록 유도)
- S기에 한 번씩 복제되면서 세포 당 약 50~100개 정도의 DNA가 됨
- 감염된 상피세포가 각질 형성 세포로 분화되면 후기 RNA가 전사됨
- DNA 수가 수천 개 이상으로 복제되고 캡시드가 핵에서 조립된 후 세포를 파괴하고 방출 (바이러스가 세포를 파괴하고 방출되면서 세포가 죽음 → 양성 종양
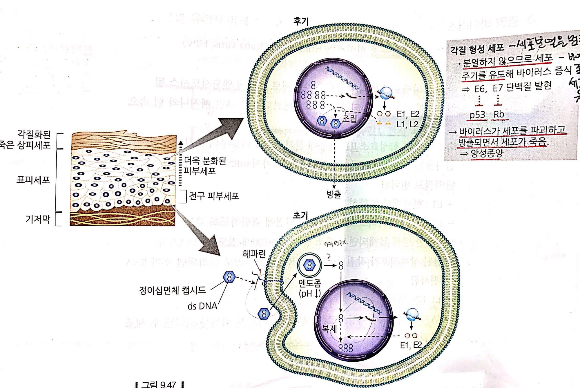
(ㄴ) 암 발생 기작
- 각질 형성 세포 : 더 이상 직접 체세포 분열을 하지 않음 -> 바이러스가 자기 증식을 하기 위해 E6, E7 단백질을 합성해서 숙주 세포의 복제를 유도 (E6 : 유비퀴틴화를 통해 p53의 분해를 촉진, E7 : Rb에 E2F 대신 결합해서 E2F가 전사 인자로 작용할 수 있도록 함)
- 바이러스 DNA가 우연히 숙주세포의 염색체에 삽입될 경우, 캡시드와 조립해 바이러스 입자로 방출되지 못하고 계속 숙주세포의 분열을 유도하면서 암을 유발


(ii) RNA 바이러스 - 라이스 육종 바이러스 (RSV) : 레트로 바이러스 ( HIV도 이러함)
- 닭에게 종양을 일으키는 바이러스 - 라우스, 1911년 발견
- 피막 : SU, TM의 두 가지 당단백질 존재
- 캡시드 : 정이십면체 구조
- 캡시드 내에 동일한 두 분자의 (+) RNA의 핵산이 뉴클레오 캡시드 형태로 존재
- 역전사 효소, 삽입 효소, 단백질 분해 효소가 들어 있어 바이러스가 숙주 내에서 증식할 수 있도록 도와줌
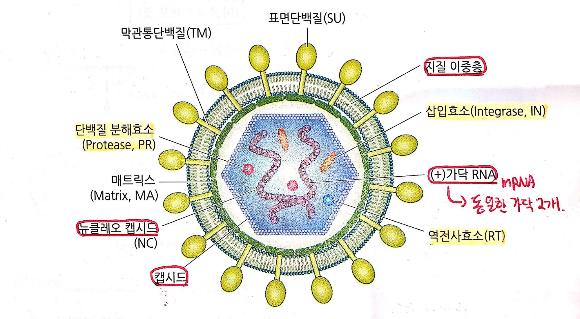
(ㄱ) 생활사
- 세포막의 특이 수용체에 부착 후, 세포막과 피막이 직접 융합되어 캡시드만 세포 내로 진입
- 캡시드 틈으로 dNTP가 유입되면서 캡시드 내에서 RT에 의한 역전사 과정 진행 : (+) RNA가 이중가닥의 cDNA로 바뀜
- 분열 중인 숙주세포의 염색체로 PIC가 접근
- 삽입 효소가 cDAN 양끈의 LTR 서열을 인식해 숙주 염색체에 무작위로 삽입시킴 (프로바이러스 상태가 됨)
- 삽입된 프로바이러스의 5' LTR 내에 존재하는 프로모터로부터 전사가 일어남 (선택적 스플라이싱 과정을 통해 두 가지 mRNA를 합성)
- 세포막 근처에서 캡시드 구조가 조립됨
- 조립과 동시에 세포 밖으로 방출되면서 숙주 세포막을 감싸 피막 구조를 획득

(ㄴ) 암 발생 기작
- 조상 RSV가 숙주 염색체에 무작위로 끼어들어 증식하던 중 우연히 c-src(숙주세포의 세포 신호 전달 과정을 매개) 유전자 곁으로 삽입됨
- 바이러스 입자가 방출되는 과정에서 c-src 유전자를 함께 지니고 나옴
- 유전자 내에서 c-src의 활성을 조절하는 조절 도메인이 결실됨 (c-src : 정상 유전자 v-src : 발암 유전자)
- v-src를 지닌 현재의 RSV가 숙주세포에 감염되면 v-src로부터 번역된 단백질이 계속 세포 분열 신호를 전달해서 암세포로 증식

함께 보면 도움이 되는 글 보러가기
세포 분열
1. 체세포 분열 - 세포는 적당한 크기로 유지되도록 조절을 통해 자신의 내용물을 복제한 후 둘로 나누어집니다. - 유전물질의 증폭, 유전물질 분배, 세포질 분열 이 3 단계로 이루어집니다. 진핵 생물의 DNA 구조..
atoa00.tistory.com
세포 괴사와 세포 사멸의 차이
세포 괴사 (Necrosis) VS 세포 자살 (Apoptosis) 세포 괴사 세포 자살 자극 물리적 자극 (상처) 유전적 신호 ( 단백질 활성화, 전사와 번역 유발) 세포 구조 소기관, 세포막 파괴 염색질 응축, 세포막 파괴없이 기..
atoa00.tistory.com